2017-05-30
ボストン・サイエンティフィック、2017年第1四半期決算発表
ボストン・サイエンティフィック(本社:マサチューセッツ州マールボロ、NY 証券取引所略号: BSX)は本日(2017年4月27日)、2017年3月31日締め第1四半期の売上高が21億6,000万ドルになったことを発表しました。売り上げは、財務報告ベース、為替変動の影響を除く実質ベース共に前年同期比で10%上昇しました。当四半期の利益はGAAPベースでは2億9,000万ドル(前年同期は2億200万ドル)、1株当たり利益(EPS)は0.21ドル(前年同期は0.15ドル)を計上しました。1株当たり修正後利益は0.29ドル(前年同期は0.28ドル)に達しました。
ボストン・サイエンティフィック社長兼CEOのマイク・マホーニーは次のように述べています。
「第1四半期は、多岐にわたる事業分野、そして様々な地域のいたるところで素晴らしい成長が見られ、喜ばしい業績でした。また、当社は、1株当たり修正後利益の2桁成長の継続を目指しながら、自社のカテゴリーリーダーシップ戦略を強化するイノベーションに投資しています。」
第1四半期業績と主な取り組み
- 第1四半期の売上高は21億6,000万ドルを達成。当社発表の予想レンジは20億5,000万~21億ドル。財務報告ベースおよび実質ベース共に前年同期比10%の増加。
- 既存ビジネスの第1四半期成長率は前年同期比9%の増加(為替変動の影響およびエンドチョイス社(EndoChoice Holdings, Inc.)の買収による売上を除く)。
- GAAPベースでは、1株当たり利益0.21ドル(当社予想では0.18ドル~0.21ドル)。修正後の1株当たり利益は0.29ドル(当社予想では0.29~0.31ドル)。2月に販売および臨床から自主撤退したLotus™バルブ1関連費用を含む。
- 第1四半期は全事業部門で前年同期比売上増を達成。部門別内訳は以下のとおり。
o メドサージ部門:報告ベースおよび実質ベースの成長率15%、既存ビジネス成長率12%
o カーディオバスキュラー部門:報告ベース、実質ベース、既存ビジネスの成長率8%
o リズムマネジメント部門:報告ベースの成長率7% 、実質ベースおよび既存ビジネスの成長率8%
- 地域別でも好調な前年同期比売上増を達成。内訳は以下のとおり。
o 米国:報告ベースおよび実質ベースの成長率13%、既存ビジネス成長率11%
o 欧州:報告ベースの成長率2%、実質ベースおよび既存ビジネスの成長率7%
o AMEA(アジア太平洋、中東、アフリカ):報告ベースの成長率9%、実質ベースおよび既存ビジネスの成長率8%
o 新興国市場2:報告ベース、実質ベース、既存ビジネスの成長率12%
- 様々な病状や心構造に対応する多様な経カテーテル大動脈弁植込み(TAVI)デバイスを心臓内科医および心臓外科医に提供するため、低侵襲TAVIデバイスに集中した心構造疾患治療用機器を取り扱うスイスの株式非公開会社であるシメティス社を、4億3,500万ドルの現金で買収する正式契約を締結。
- 英国国立医療技術評価機構(NICE)が、心不全治療の際に、ボストン・サイエンティフィックの、EnduraLife™バッテリーを搭載した両室ペーシング機能付き植込み型除細動器(CRT-D)の使用を推奨し、さらに、バッテリー寿命を延ばすと、回避できる置換手術の数を減らせると考えられるため英国の国民健康保険システムにおいて5年で600万ポンド削減できる可能性があると注記したことを発表。
- 欧州においてCRT-D3のRESONATE™シリーズのCEマークを取得し、発売することにより、SmartCRT™およびEnduraLifeバッテリーを搭載した新たな心不全治療用機器を医師に提供。
- 米国心臓病学会学術集会において、3年間のEVOLVE Ⅱ試験の結果を発表し、SYNERGY™生体吸収性ポリマ搭載ステントの安全性の高さ、特に、機器植込み手術の24時間後を経過してから3年後までのステント血栓症(ST)発生率(0.2%)が非常に低いことを強調。
- 当社のEluvia™薬剤溶出型末梢血管ステント4とZilver™ PTX薬剤被覆型ステント(Cook Medical社製)を直接比較するIMPERIAL試験に465名の患者登録を完了。データは、米国の規制承認申請書類の資料として使用予定。
- Ranger™パクリタキセル被覆PTAバルーンカテーテル4について2つの臨床段階を達成。一次開存率が高く、標的病変の血行再建手術が発生しなかったことを立証した12カ月の試験結果をチャリングクロス・シンポジウムで発表。RANGER II SFA試験の登録を開始し、米国および日本における規制承認申請の資料とする予定。
- WATCHMAN™左心耳閉鎖(LAAC)デバイスの2つの治験の患者登録を開始。ASAP TOOは、ワルファリンを投与できない患者における上記デバイスの使用について評価する試験で、米国における表示拡大につながる可能性。SALUTEは、特に日本での規制承認を求めて計画。
- Lotusバルブは現在、使用または販売されていません。
- 「新興国市場」の定義について:各国の経済状況、医療部門の状況、および当社の国際経営力を考慮の上、高い成長性を持つと当社が判断した国々を「新興国市場」と定義しています。現時点では20カ国がこの定義に該当します。
- CEマーク取得。CRT-DのResonateシリーズは、米国では使用または販売されていません。
- Eluvia薬剤溶出型末梢血管ステントおよびRangerパクリタキセル被覆PTAバルーンは、CEマーク取得済です。米国では、これらは治験用医療機器であり、米国の法律により治験目的の使用のみに制限され、販売されていません。
第1四半期の純売上高
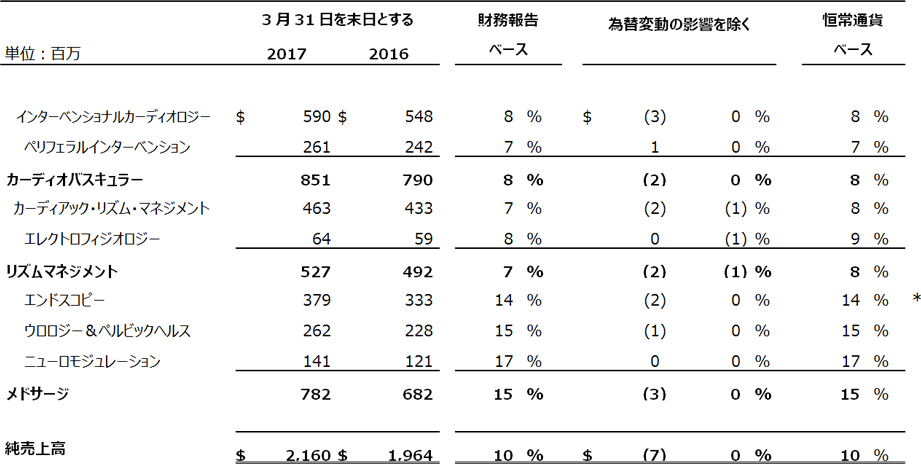
成長率は四捨五入していない実数値であり、再計算する際に誤差が生じる場合があります。
売上成長率は、外国為替の変動による影響および/または多額の売上を伴う最近の買収の影響を除いたものであり、米国のGAAP(一般会計原則)に従って作成されていません。ボストン・サイエンティフィックがこうした非GAAPの数値を使用する理由につきましては、本プレスリリースに添付の別紙をご覧ください。
現在予想される2017年第2四半期の売上は21億8,500万~22億1,500万ドルの範囲で、財務報告ベースでは前年同期比およそ3~4%増、エンドチョイスによるおよそ70ベーシスポイントの貢献を含めた実質ベースでは前年同期比およそ5~6%増になる見込みです。GAAPベースの利益は、1株当たり0.18~0.21ドルの範囲になる見込みです。買収関連、組織再編および組織再編関連の純費用、さらに減価償却費用を除いた調整後利益は、1株当たり0.30~0.32ドルの範囲になる見込みです。
ボストン・サイエンティフィックについて
将来予測に関する記述についての注意事項
このような相違をもたらす可能性のあるリスクや不確実要素の例として、将来の経済、政治、競争、医療費償還および法規制の条件、新製品導入、市場における新製品受容、製品市場、市場の価格動向、予想される手術件数、企業・事業の買収や統合、臨床試験結果、人口統計学的動向、知的所有権、訴訟、金融市況、組織再編プログラムの実施とその効果、当社経営戦略(コスト削減計画・成長計画を含む)の実施とその効果、当社および競合他社の将来的な経営上の意思決定などがあります。新たなリスクや不確実要素は随時発生の可能性があり、予測が困難です。これらの要因すべてを正確に予測することはほとんど不可能であり、その多くは当社の制御の及ばないものです。当社の将来的な経営に影響する可能性のあるこれらの要因およびその他の重大なリスクの一覧およびその詳細説明につきましては、米国証券取引委員会に提出した最新の10-K 年次報告書パート I 1A 項目「危険因子」をご参照ください。なお、この内容は、提出済みもしくは今後提出する10-Q 四半期報告書パート II 1A 項目「危険因子」で更新される場合があります。本プレスリリース発行後に当社の予測に変化が生じた場合、または予測の根拠となった事象、条件、状況に変化が生じた場合、または将来予測と実際の結果に相違をもたらす原因となる変化が生じた場合においても、当社は将来予測に関する記述内容を公開の場で更新または改訂する予定はなく、その義務を一切否認します。本注意事項は本プレスリリースに記載された将来予測に関するすべての記述に適用されます。
非GAAPによる財務情報の使用
連絡先:
メディア関連 : ケリー・リーダム
508-683-5543 (オフィス)
メディア・リレーションズ
Boston Scientific Corporation
kelly.leadem@bsci.com
投資家関連 : スーザン・リサ, CFA
508-683-5565 (オフィス)
投資家向け情報担当
Boston Scientific Corporation
investor_relations@bsci.com