WATCHMAN FLX™
Dispositivo para Cierre de la Orejuela Auricular Izquierda
Construido a partir del dispositivo para LAAC más estudiado y más implantado del mundo, WATCHMAN FLX™ es una alternativa probada a la terapia1 OAC a largo plazo para la reducción del riesgo de accidente cerebrovascular en pacientes con fibrilación auricular no valvular.
WATCHMAN FLX™ se estudió en el Ensayo Clínico PINNACLE FLX US IDEC. El estudio fue diseñado para establecer la seguridad del procedimiento y la eficacia del cierre del dispositivo para LAAC de nueva generación, WATCHMAN FLX™.
Videos

PRESENTACIÓN DE ÚLTIMA HORA DEL PINNACLE FLX
Evaluación Principal de Resultados del Dispositivo para LAAC de Última Generación: el Ensayo PINNACLE FLX
Presentado por el Dr. Shephal K. Doshi
Mayo 8, 2020
CIENCIA HRS 2020
Estudio Clínico PINNACLE FLX
Diseño del estudio
- Ensayo no aleatorio de 400 pacientes, 29 lugares en EE.UU., de un solo grupo, que evalúa el WATCHMAN FLX para determinar la no inferioridad con respecto a los objetivos de rendimiento de seguridad y eficacia basados en el dispositivo WATCHMAN™.
- Seguimiento: 45 días (+ TEE), 6 meses, 12 meses (+ TEE), 18 meses y 24 meses.
- Características del Paciente: CHA2DS2-VASc promedio de 4.2 ± 1.5, HAS-BLED promedio de 2.0 ± 1.0.
- Régimen Farmacológico Posterior al Implante: NOAC/ASA durante 45 días, Clopidogrel/ASA hasta 6 meses, ASA posterior a los 6 meses.
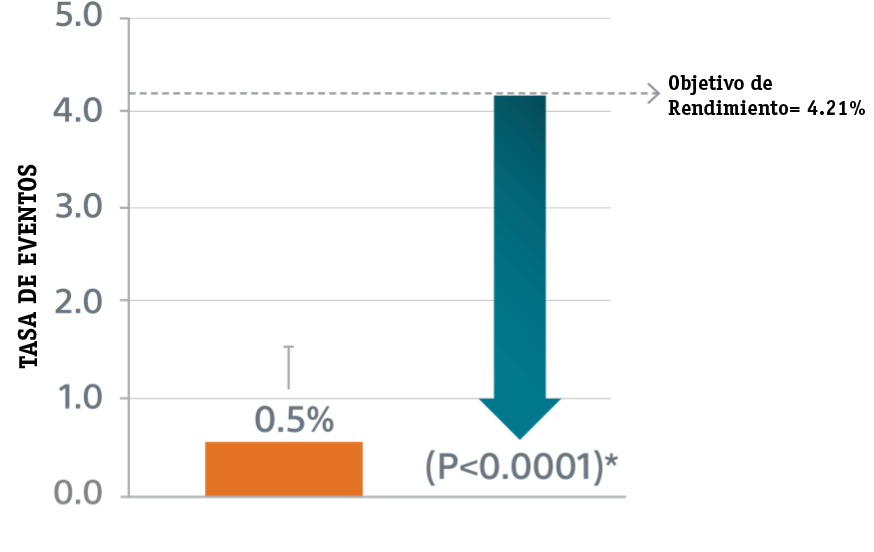
- Criterio de Valoración Principal de Seguridad: muerte por cualquier causa, accidente cerebrovascular isquémico, embolia sistémica o eventos adversos relacionados con el dispositivo o el procedimiento que requieran cirugía o intervención endovascular importante dentro de los 7 días posteriores al procedimiento o al momento del alta hospitalaria, cualquiera que sea el caso.
- Criterio de Valoración Principal de Eficacia: la tasa de cierre efectivo de la OI definida como cualquier flujo de un peridispositivo ≤5 mm demostrado por TEE a los 12 meses.
- Criterio de Valoración Secundario de Eficacia: la aparición de accidente cerebrovascular isquémico o embolia sistémica a los 24 meses desde el momento del enrolamiento.
- Los criterios de inclusión/exclusión son consistentes con los criterios de inclusión/exclusión del estudio clínico del WATCHMAN. Los pacientes deben ser elegibles para NOAC a corto plazo frente a la warfarina en estudios clínicos previos.
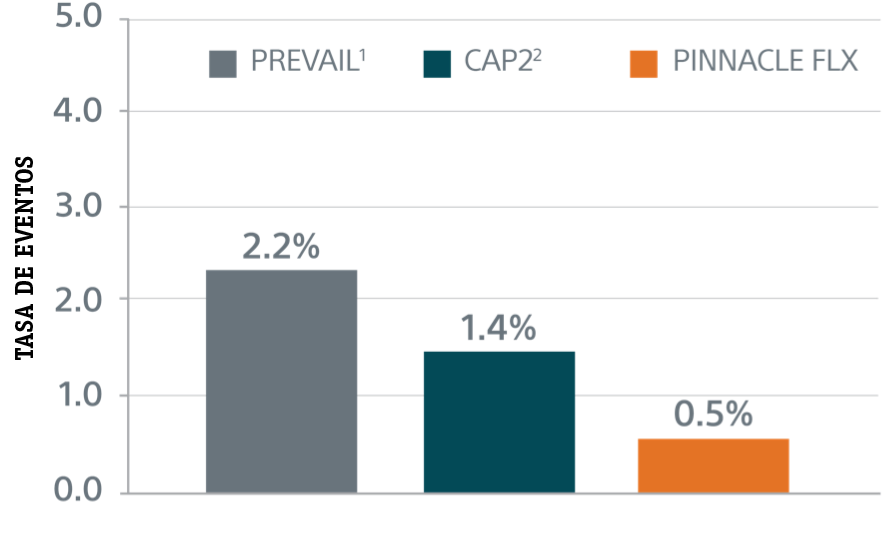
Criterios de Valoración Principales de Seguridad

Criterios de Valoración Principales de Eficacia
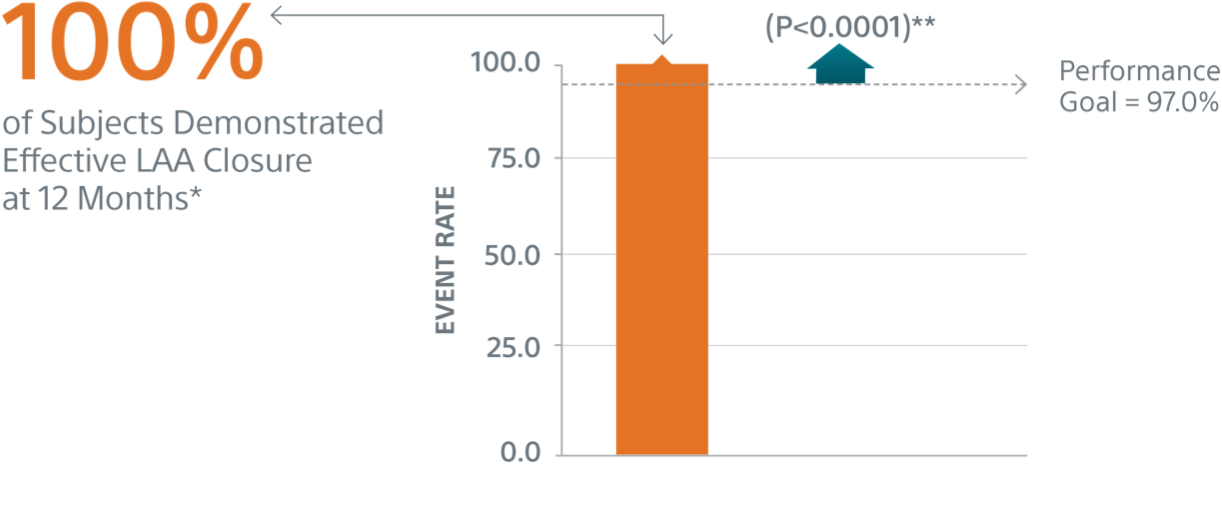
** Objetivo de Rendimiento basado en las tasas observadas en PREVAIL(1) y CAP2(2), menos un delta clínicamente relevante.
Diseñado para Tratar la Más Amplia Gama de Anatomías en Pacientes
Los tamaños del WATCHMAN FLX™ van desde (20 mm - 35 mm)


NOTICIA EXCLUSIVA:
Discusión del Ensayo Clínico PINNACLE FLX
Dr. Kenneth Stein, Senior Vice President, Chief Medical Officer, Rhythm Management at Boston Scientific
Dr. Ian Meredith, Executive Vice President, Global Chief Medical Officer, Boston Scientific
Dr. Ian Meredith, Executive Vice President, Global Chief Medical Officer, Boston Scientific