ELUVIA ™
Sistema de stent liberador de medicamentos
El Sistema de Stent Liberador de Fármacos Eluvia mostró resultados SUPERIORES en el primer ensayo DES SFA directo.
Estudio IMPERIAL: Un estudio multi-céntrico controlado aleatorio global con aleatorización 2:1 del Stent Liberador de Fármacos Eluvia™ contra el de diseño de no inferioridad, simple ciego de no inferioridad de laboratorio independiente Core Lab del Stent PTX™ Zilver™ PTX ™ de Cook Medical La superioridad se determinó en un análisis post hoc que se especificó antes del desenmascaramiento. Tasa de permeabilidad primaria a 12 meses de 86.8% en el brazo Eluvia vs. 77.5% en el brazo Zilver PTX (valor p = 0.0144).
Objetivo
Diseño del Estudio IMPERIAL
Multi-céntrico global, aleatorización 2:1, contra ensayo de no inferioridad, simple ciego, controlado de Stent PTX™ Zilver™ de Cook Medical, de laboratorio independiente Core Lab.
- 465 (RCT) pacientes en 64 centros
- Seguimiento a 5 años
- Grado de Estenosis ≥ 70% (Evaluación angiográfica visual)
- Diámetro del vaso ≥ 4 mm y ≤ 6 mm
- Longitud total de lesión ≥ 30 mm y ≤ 140 mm
Características al Inicio del Estudio
| CARACTERÍSTICAS DE LOS PACIENTES | ELUVIA™ (n=309) |
Zilver PTX™ (n=156) |
|---|---|---|
| Edad (Años) | 68.5±9.5 | 67.8±9.4 |
| Género Masculino | 66.0% | 66.7% |
| Diabetes Mellitus | 41.7% | 43.6% |
| Consumo de cigarrillo | 86.1% | 84.0% |
| CARACTERÍSTICAS DE LA LESIÓN | ELUVIA™ (n=309) |
Zilver PTX™ (n=156) |
|---|---|---|
| Longitud de lesión Objetivo (mm) | 86.5±36.9 | 81.8±37.3 |
| Muy Calcificada | 40.1% | 32.3% |
| Oclusiones Totales | 31.2% | 30.3% |
| Extendiéndose en SFA Distal | 66.3% | 65.4% |
Resultados de Patencia Primaria a 12 Meses
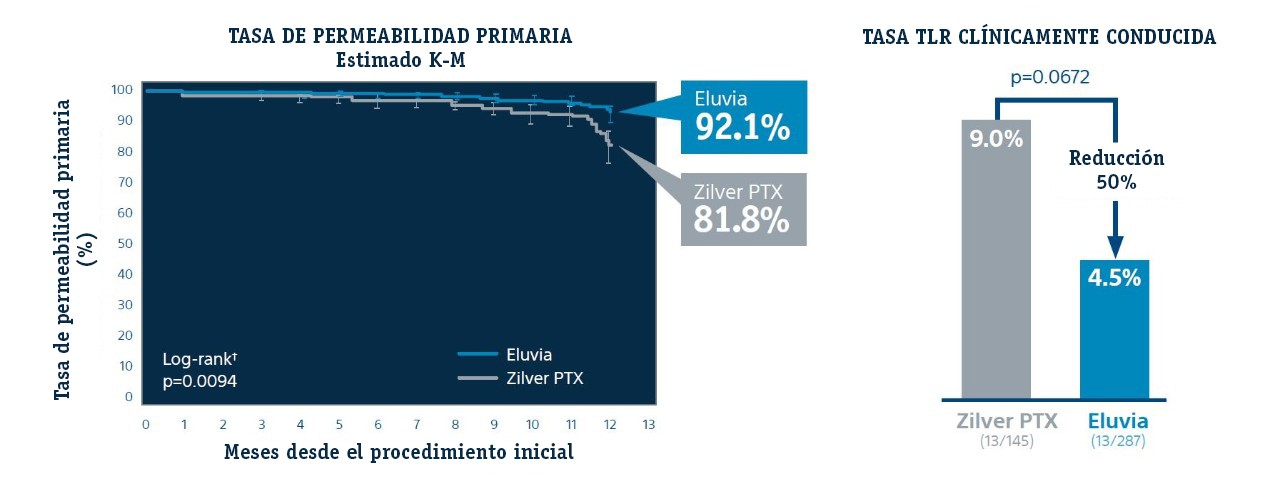
* Estimación de Kaplan Meier; la permeabilidad primaria determinada por la relación de velocidad sistólica máxima (PSVR) de ultrasonido dúplex (DUS) es ≤ 2.4 en consulta de seguimiento de 12 meses, en ausencia de TLR clínicamente conducido o bypass de lesión objetivo.
** Gray, WA TCT 2018.
† El valor p de rango logarítmico compara todas las curvas K-M desde el tiempo cero hasta la ventana de seguimiento completa a un año.
1. Ensayo IMPERIAL: Un ensayo multi-céntrico controlado aleatorio global con aleatorización 2:1 del Stent Liberador de Fármacos Eluvia™ contra el de diseño de no inferioridad, simple ciego de no inferioridad de laboratorio independiente Core Lab del Stent PTX™ Zilver™ PTX ™ de Cook Medical. La superioridad se determinó en un análisis post hoc que se especificó antes del desenmascaramiento. Tasa de permeabilidad primaria a 12 meses de 86.8% en el brazo Eluvia vs. 77.5% en el brazo Zilver PTX (valor p = 0.0144).
















